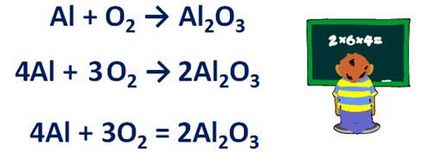kémiai egyenletek
Lecke 27. Kémia Grade 8
Áttekintés leckét „kémiai egyenlet”
Alapján a törvény tömegmegmaradás anyagok alkotják egyenlet kémiai egyenlet reaktsiy.Himicheskoe - felvétel feltételes kémiai reakció kémiai képlet és jelölés.
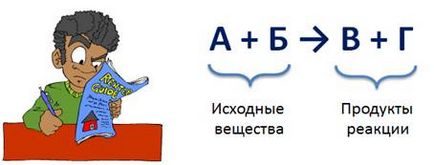
A bal oldalon az egyenlet van írva általános képletű, vagy általános képletű anyagok, amelyek lépett kémiai reakció. Ezek az úgynevezett prekurzor. közötti „plusz” jel a jobb oldalon az egyenlet van írva az általános képletű, vagy a képlet a reakció termékek. azaz képződő anyagok közötti reakció őket is fel a jel „plusz”, és a bal és jobb oldali része az egyenletnek tesz a nyíl.
A kémiai reakció lehet a következő egyenlet szemlélteti molekuláris. Ie molekuláris egyenlet - az egyenlet, amelyben a kiindulási anyagok és a reakció termékek kerülnek rögzítésre formájában molekulák. Ha csapadék képződik a reakcióban. a jobb mellé tegye le nyíl (↓), és ha gáz keletkezik. majd közvetlenül mellette fel nyíl (↑).
A felvétel után nahodyatkoeffitsienty egyenlet rendszert. azaz számadatok néző képletek anyagok az atomok számát előtt és után a reakcióelegyet azonos volt.
Például, tudjuk írni az egyenletet a reakció a hidrogén és oxigén. Kezdetben azt is jelezzük, a képlet anyagok léptek kémiai reakció - jelentése hidrogén (H2) és az oxigén (O2), állítsa közötti „plusz” jel, a reakciójával kialakított víz - H2 O. között anyag bal és jobb oldalán a nyíl készlet. Lássuk, hány hidrogénatomok a bal és jobb oldalán. Két hidrogénatom kapunk előtt és után a reakció, és az oxigénatom, hogy a reakció 2, a reakció után - atom. Ezért, a jobb oldalon megadott képlet, mielőtt a víz 2 faktorral De most a jobb oldalon az egyenlet 4 lett hidrogénatom, és a bal oldalon csak 2. Annak érdekében, hogy kiegyenlítse a hidrogénatomok számát szükséges a bal elülső hidrogén ellátási 2. Mivel az együttható mi megegyezett a szám minden atom a bal és a jobb oldalon az egyenlet, ma már egyre nem egy nyíl és egy egyenlőségjel.
A helyes kiválasztását együtthatók az egyenletben a reakció kell végezni több tényező:
Mielőtt · képlet egyszerű anyagok rögzítésére képes frakcionált tényező. Például, a reakciót a bután égő:
C4 H10 O2 → CO2 + H2O + CO2 előtt meghatározott képlet faktor 4, mivel képletű 4 szénatomos, hogy víz arány által meghatározott általános képletű 5, mint reagáltatunk egy 10 hidrogénatomok. A reakcióval 13 oxigénatomot és legfeljebb 2 atom reakciót, azt jelenti, hogy a kínálat a szükséges oxigén formula faktor 6,5. És mivel az együttható azt mutatja, nem csak a száma az atomok és molekulák, de szükséges, hogy dupla arány egyenlet. Tehát az egyenlet a következő lenne: 2C4 H10 + 13O2 → 8SO2 + 10N2 kb.
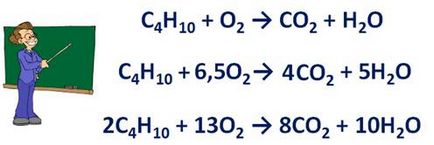
· Ha a reakcióvázlatban egy só, az első egyenlővé az ionok száma a sóképzést. Például, a reakciót foszforsav és kalcium-hidroxid képződött só - kalcium-foszfát és a víz.
H3 PO4 + Ca (OH) 2 → Ca3 (PO 4) 2 + H2 O. Ez a sót, amely foszfát-ionok egy töltés 3- és kalcium ionok egy 2+ töltést. Kiegyenlítés számuk meghatározása előtt képletű 2 tömegarány a foszforsav és a kalcium-hidroxid, hogy a általános képletű - 3 arányt.
· Ha a reakcióvázlatban vannak atomok a hidrogén és oxigén, az első kiegyenlített hidrogénatomok, és akkor is csak az oxigén. A korábbi rendszer azt mutatja, hogy a bal oldalon a 12 egyenlet hidrogénatomok a helyes - 2 csak azt jelenti, hogy mielőtt a vizet, hogy a képlet kell együttható 6. Számítsuk ki az oxigénatomok számának. Amíg a reakció 14, a reakció után is lehetséges, ahelyett 14. Ezért a nyíl egyenlővé.
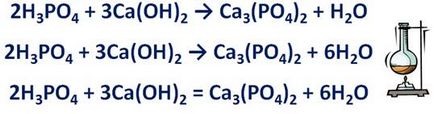
· Ha a reakció során számos képletek sók, meg kell kezdeni hangszínkiegyenlítést ionokkal a só, amely több közülük. Például, a reakciót a bárium-nitrátot és alumínium-szulfát-só képződött két - bárium-szulfát és alumínium-nitrát. A legnagyobb számú ionok sót tartalmaz - alumínium-nitrát, azonban először szükséges, hogy kiegyenlítse a ionokat, ami úgy alakul ki ezt a sót, azaz, alumínium-ionok és nitrát ionokat. Ba (NO 3) 2 + Al2 (SO4) 3 → BaSO4 + Al (NO3) 3. Alumínium töltés 3+ ionok nitrát - 1-. Ezért, a megállapított együttható 3. Mielőtt a képlet Al2 (SO4) 3-nak kell szállítani az együttható 1 a bal oldalon az egyenlet a következő képlet Ba (NO 3) 2, de ez nincs hozzárendelve. Kiegyenlíti a fennmaradó ionok. Bárium ionok a reakcióelegyhez 3, a reakciót követően 1, ezért mielőtt BaSO4 meghatározott képlet 3 arányban, nitrát ionokat reakció előtt 6, így a jobb első Al (NO3) 3 arány beállítása 2. A számú alumínium atomok ugyanazt a reakciót és után, a T .e. 2. bárium-ionok és szulfátionok reakció előtt, és a reakció után egyaránt - 3.
· Ha a atomok száma az elem egy darabból is egyenletet rendszert, és a másik páratlan, szükséges formula páratlan számú atomok szállít egy tényező a 2, majd egyenlővé a száma az összes atom. Például, hogy helyezze a együtthatók a reakcióban alumínium oxigénnel. Al + O2 → Al2 O3. A reakciót kialakítva alumínium-oxid - Al2 O3. A oxigénatomok számának hogy a reakció még, azaz két, és páratlan a reakció után - 3. Ezért, mielőtt az alumínium-oxid által meghatározott képlet 2 faktorral Ennek eredményeként lettünk 6 oxigénatomot, a reakció után, azt jelenti, a bal oldalán a képletet, hogy az oxigén együttható beállítva 3. Kezdje, hogy kiegyenlítse a számát alumínium atomok és legfeljebb a reakció után. Reakció előtt 1 atom a reakció után - 4. Ezért, a bal oldalán a általános képletű alumínium arány beállításához 4. Most az atomok számát az egyes kémiai elem a bal és jobb oldalon az egyenlet egyformán áramkört, és a nyíl kell helyett ugyanolyan jel.